近日,中国科学院合肥物质院健康所刘青松药学团队研发出一种新型受体相互作用蛋白激酶1(RIPK1)抑制剂,为程序性坏死(necroptosis)相关炎症性疾病的治疗提供了新的候选药物。该研究成果发表于药物化学领域权威期刊Journal of Medicinal Chemistry。
研究表明,炎症性肠病(IBD)和全身性炎症反应综合征(SIRS)等炎症性疾病的发病机制与程序性坏死密切相关。当细胞发生程序性坏死时,细胞膜破裂并释放出大量细胞损伤相关物质,诱发炎症反应。RIPK1-RIPK3-MLKL信号轴被认为是程序性坏死的核心通路,其中RIPK1是该通路的关键调节蛋白。因此,抑制RIPK1的激酶活性成为治疗相关炎症性疾病的潜在策略。
研究团队前期通过药物重定位策略,发现处于临床阶段的FGFR抑制剂AZD4547能够通过抑制RIPK1发挥抗程序性坏死作用,并在小鼠SIRS模型中验证了其治疗效果(Acta Pharmacologica Sinica, 2023, 44(4):801-810)。在此基础上,研究人员以AZD4547的骨架为起点,结合计算机辅助药物设计和Ⅱ型激酶抑制剂设计策略,通过系统的构效关系研究和结构优化,获得了新型1H-吡唑-3-胺衍生物44。在体外活性测试中,该化合物具有显著的RIPK1抑制活性(IC50 = 5.33 nM),并在219种蛋白激酶的广谱筛选中表现出优异的选择性。在TSZ诱导的人类及小鼠细胞模型中,化合物44可以有效阻断程序性坏死。此外,该化合物以剂量依赖方式抑制RIPK1及其下游RIPK3和MLKL的磷酸化。药代动力学研究表明,化合物44在大鼠和小鼠上具有良好的口服生物利用度,且展现出较高的血液暴露量。进一步体内研究发现,在TNF-α诱导的SIRS模型中,口服化合物44(10 mg/kg)能有效阻止小鼠体温下降并提高存活率;在DSS诱导的IBD模型中,其可以有效减轻结肠缩短和炎症损伤。综上所述,化合物44作为一种高活性、高选择性且具有良好成药性的新型RIPK1抑制剂,展现出显著的抗炎潜力,是具有进一步开发价值的候选药物。
该研究工作获得了国家自然科学基金、安徽省科技重大专项和安徽省重点研发计划等项目的支持。
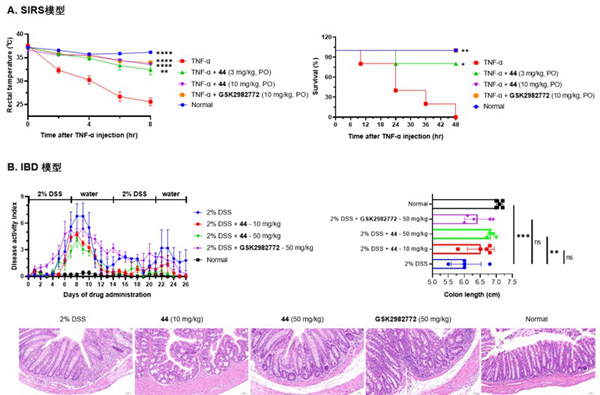
化合物44在多种炎症性疾病动物模型中的治疗效果
文章链接:https://doi.org/10.1021/acs.jmedchem.5c02124
转载自:https://www.hf.cas.cn/kxyj/kyjz/202511/t20251120_8014918.html


