特发性肺纤维化(IPF)是一种预后极差的肺间质性疾病,除肺移植外,尚无有效手段逆转纤维化肺部、修复损伤肺功能。近年来研究证实,具有多向分化潜能的间充质干细胞(MSCs)可以通过旁分泌和免疫调节功能干预IPF的发展,有望成为该疾病的“突破性疗法”。但是,由于缺乏合适的干细胞活体示踪手段使得体内治疗机制研究受限。与此同时,移植干细胞的低存活率导致的体内治疗稳定性差进一步限制了干细胞疗法的临床转化。
在新型纳米材料用于干细胞CT成像示踪及干细胞功能调控研究前期工作基础上(Biomaterials 2022, 121731; Biomater. Sci. 2022, 10, 368-375; Nanomedicine: NBM, 2022, 41),中国科学院苏州纳米技术与纳米仿生研究所张智军研究员等设计了一种超氧化物歧化酶(SOD)工程化的金纳米粒子组装体(SOD@Au NS),用于移植MSCs在治疗IPF过程中的抗氧化保护和CT成像示踪。所构建的SOD@Au NS可以克服天然酶稳定性差和穿膜能力弱的问题,其优良的活性氧(ROS)清除功能可有效提升MSCs在肺纤维化环境中的抗氧化损伤能力,增强其在炎症微环境下的存活,从而显著改善对IPF的治疗效果。同时,研究发现,SOD@Au NS作为CT成像造影剂,可以对移植MSCs体内分布、存活与迁移等进行实时监控(图1)。
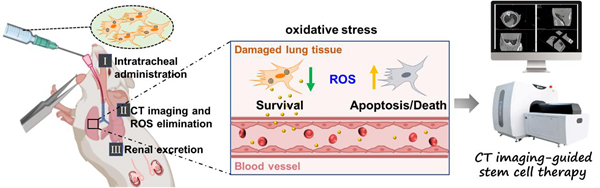
图1. SOD@Au NS用于移植MSCs抗氧化保护和CT成像示踪示意图
如图2a所示,SOD@Au NS标记的MSCs移植到IPF小鼠肺部后,可以通过CT成像技术实现移植干细胞18天内的体内分布和迁移等信息的可视化追踪,为阐明干细胞治疗IPF的机制研究提供了重要的依据。由于SOD@Au NS的ROS清除能力,生物发光成像(图2b)证明标记的MSCs在炎症微环境中的存活能力有了明显的提高,从而增强了对IPF的修复效果。
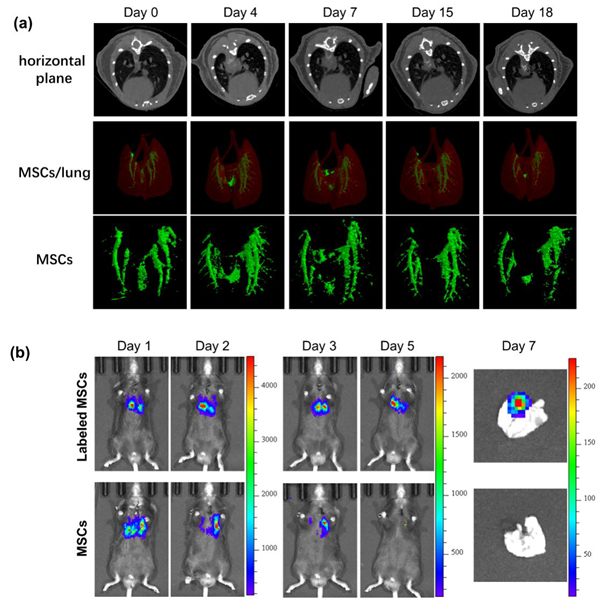
图2. (a)SOD@Au NS标记的MSCs在IPF治疗中18天内的CT成像示踪图及(b)生物发光成像图
上述成果近期以SOD-Functionalized gold nanoparticles as ROS scavenger and CT contrast agent for protection and imaging tracking of mesenchymal stem cells in Idiopathic pulmonary fibrosis treatment为题在国际学术期刊Chemical Engineering Journal在线发表。苏州纳米所博士后虞成功为第一作者,黄洁副研究员和张智军研究员为共同通讯作者。相关工作得到国家自然科学基金、中科院国际合作项目和江苏省卓越博士后项目等支持。
